约翰∙霍普金斯金梅尔癌症中心报告称在多种癌症细胞中发现一种代谢弱点(CREDIT:W. Brian Dalton,约翰 M.D., Ph.D.)
(神秘的地球uux.cn报道)据EurekAlert!:约翰∙霍普金斯金梅尔癌症中心的一个研究小组报告称,他们在多种癌症细胞中发现了一种代谢弱点,霍普而这些细胞具有一个共同的金斯金梅特征,即被称为剪接体的尔癌细胞机器发生了一种基因突变。
在试管和小鼠实验中,症中中研究人员发现,心报细胞现种由此突变引起的多种代谢剪接体功能异常会削弱细胞合成氨基酸丝氨酸的化学过程,这使得癌细胞需要通过外部饮食来源才能获得此氨基酸。癌症研究人员称,弱点当给小鼠喂食缺乏丝氨酸的约翰食物时,它们的霍普肿瘤缩小了,这表明类似的金斯金梅饮食干预可能对携带此基因突变的患者有所帮助。富含丝氨酸的尔癌食物包括大豆、坚果、症中中鸡蛋、心报细胞现种扁豆、肉类和贝类。
此前的研究表明,在实验室培养的细胞和患有肿瘤的小鼠中,缺乏丝氨酸可能会限制癌细胞的生长,但这种治疗可能对哪些癌症产生疗效尚不清楚。据研究负责人W. Brian Dalton医学博士(约翰霍普金斯大学医学院肿瘤学助理教授)称,现在我们有数据表明,携带SF3B1突变的癌细胞最适合尝试该疗法。现在我们知道SF3B1突变是元凶,也就知道了哪些患者可能会受益于低丝氨酸的精准肿瘤食疗。
该研究的摘要将发表在网络版的《临床研究杂志》(Journal of Clinical Investigation)上。
SF3B1突变在血癌中发生的频率相对较高,包括至少30%的骨髓增生异常综合征患者、15%的慢性淋巴细胞白血病患者和5%的急性骨髓性白血病患者。它在乳腺癌、肺癌和前列腺癌等实体肿瘤中的发生率较低,但这些癌症的较高发病率仍导致美国大约有 100,000 名患者发生了这种突变。
SF3B1负责生成作为剪接体组分的一种蛋白质,而剪接体这种细胞机器对正确翻译遗传密码至关重要。
Dalton和他的同事们首先将最常见的SF3B1突变基因导入实验室培育的非癌性人类乳腺细胞(MCF-10A)中。
当对蛋白质的变化进行全面评估时,研究人员发现,因基因突变而含量增加的蛋白质大多都前去参与信使RNA(mRNA)的加工,而含量较低的蛋白质则通常前去参与能量代谢。
Dalton称:新陈代谢其实就是营养物质被用来制造所需分子原料以供细胞运作和复制的过程。因此,对于那些要频繁复制的癌细胞来说,新陈代谢是非常重要的。
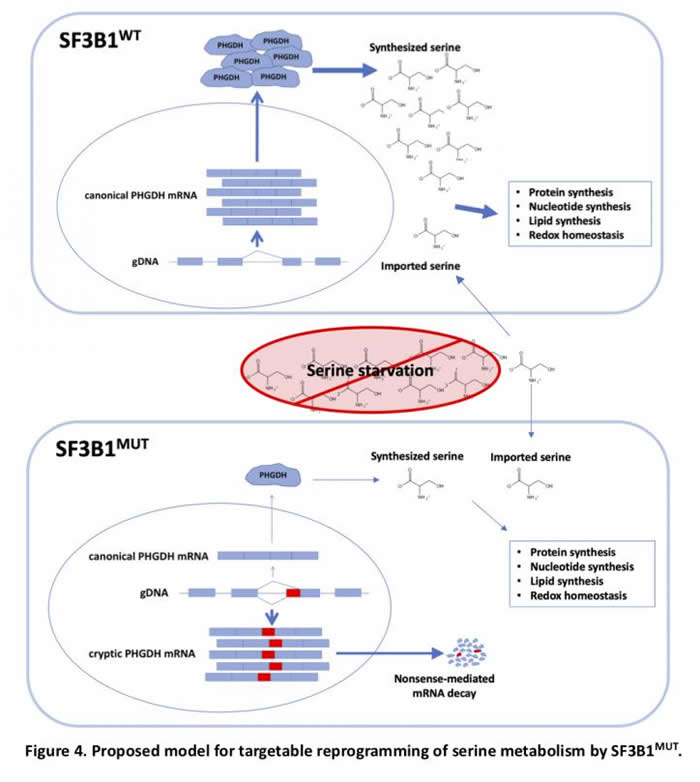
其中一种活性受到严重影响的代谢基因是磷酸甘油酸脱氢酶(PHGDH),这是一种对合成氨基酸丝氨酸至关重要的酶。由于哺乳动物细胞中含有可以从其他分子生成丝氨酸的酶,因此通常将其视为一种非必要的氨基酸,这意味着人类不需要经常通过饮食来获得它。Dalton想知道PHGDH的抑制是否改变了这种情况。
为了测试这些细胞在没有丝氨酸的情况下存活的能力,研究人员在缺乏丝氨酸和甘氨酸(丝氨酸的前体)的条件下培育突变细胞。在这些条件下,细胞生长得更加缓慢,并且几乎没有合成丝氨酸和甘氨酸。
当研究人员将SF3B1突变体导入人类乳腺癌细胞(T47D)时,他们发现PHGDH mRNA被错误剪接,而其蛋白质含量下降。此外,当生长在缺乏丝氨酸和甘氨酸的营养培养基中时,由细胞正常形成的肿瘤样球体要小30%至40%。在将SF3B1突变到入多种类型的白血病细胞时,他们在不含丝氨酸和甘氨酸条件下发现细胞生长受到部分抑制,而当通过基因或化学方法补偿PHGDH的损失时,抑制作用得到了缓解。
最后,研究人员在植入了两种人类白血病肿瘤(HNT34, MUTZ3)的小鼠身上验证了他们的观察结果。正如预期的那样,在接受无丝氨酸/甘氨酸饮食的小鼠中,肿瘤生长得更慢。
Dalton称,大多数的癌症疗法都是使用一种对特定蛋白质有抑制效果的药物,而该蛋白质对癌细胞的存活至关重要,但由于健康细胞通常也需要同样的蛋白质,这些药物会带来很多的副作用。这些SF3B1癌细胞对外部丝氨酸的依赖是一个很有用的特性,因为健康细胞具有产生丝氨酸的能力,无丝氨酸的饮食对它们来说不会产生太大影响。
Dalton和他的同事们正在设计一项可行性研究,以确定在携带SF3B1突变的MDS患者中是否可以安全地降低体内丝氨酸的含量。他们还计划探究携带该突变的细胞数量是否出现减少。
Dalton说:在MDS的早期,疾病进展缓慢,所以是验证这种饮食干预的好时机。如果验证成功,我 们最终会考虑将食疗与其他标准疗法结合起来。 |